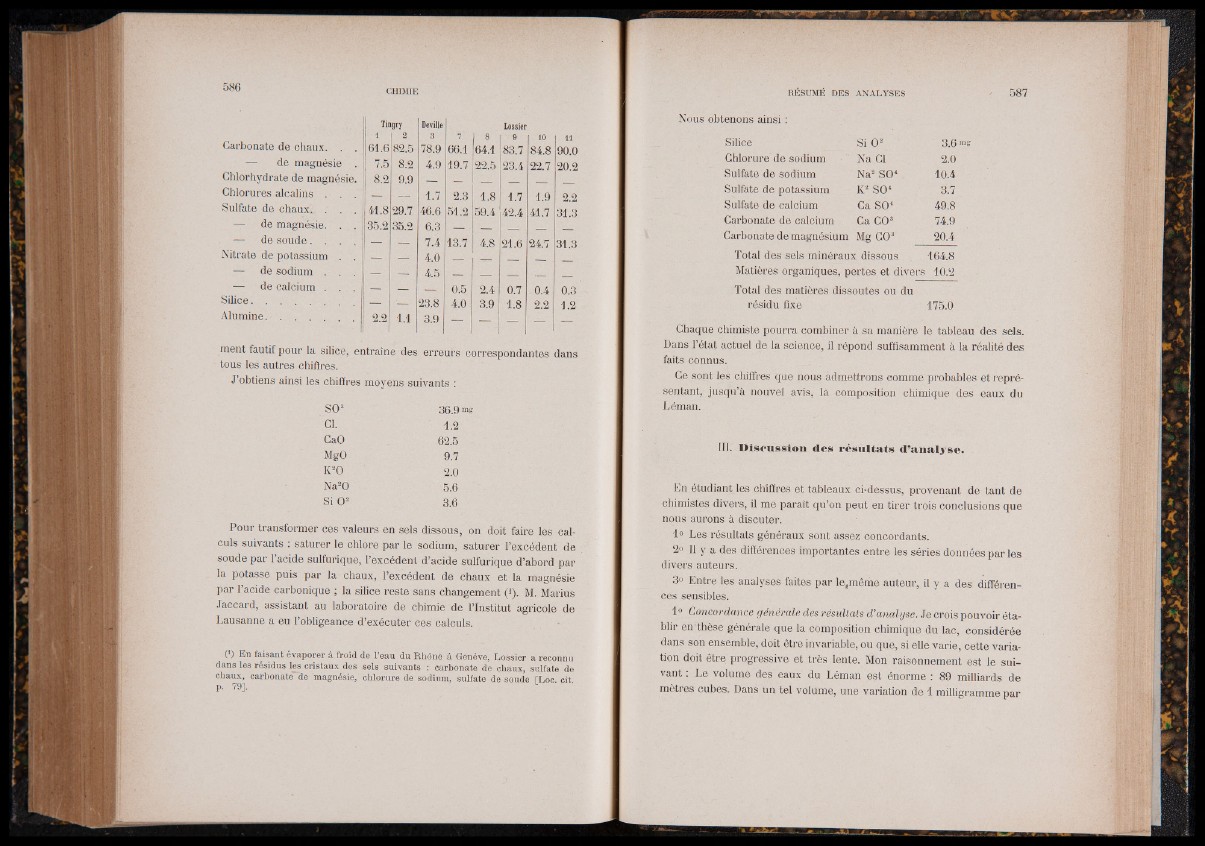
Tingry
1 W 2
Deville
3 7" 1 8
Lossier
9 10 h
Carbonate de chaux. . . 61.6 82.5 78.9 66.1 64.1 83.7 84.8 90.0
— de magnésie . 7.5 8.2 4.9 19.7 22.5 23.4 22.7 20.2
Chlorhydrate de magnésie. 8.2 9.9 '__ __L '
Chlorures alcalins . . . --- 1.7 2.3 1.8 1.7 1.9 2.2
Sulfate de chaux., . . 41.8 29.7 46.6 51.2 59.4 42.4 41.7 31.3
— de magnésie. . . . 35.2 35.2 6.3 -i. --- ____ -
— de soude. . . . B — 7.4 13.7 4.8 21.6 24.7 31.3
Nitrate de potassium . . — — 4.0 ' _ _____
— de sodium . . . — — 4.5 — pBlag§a __ '
— de calcium . . . — ■— — . 0.5 2.4 0.7 0.4 0.3
Silice. . . — 23.8 4.0 3.9 1.8 2.2 1.2
A lum in e ........................... 2 2
. '
1.1 3.9 —
"
ment fautif pour la silice, entraîne des erreurs correspondantes dans
tous les autres chiffres.
J’obtiens ainsi les chiffres moyens suivants :
so3 36.9
Cl. 1.2
CaO 62.5
MgO 9.7
K20 2.0
Na20 5.6
Si O2 3.6
Pour transformer ces valeurs en sels dissous, on doit faire les calculs
suivants : saturer le chlore par le sodium, saturer l’excédent de
soude par l’acide sulfurique, l’excédent d’acide sulfurique d’abord par
la potasse puis par la chaux, l’excédent de chaux et la magnésie
par l’acide carbonique ; la silice reste sans changement (J). M. Marius
Jaccard, assistant au laboratoire de chimie de l’Institut agricole de
Lausanne a eu l’obligeance d’exécuter ces calculs.
(’) En faisant évaporer à froid de l’eau du Rhône à Genève, Lossier a reconnu
dans les résidus les cristaux des sels suivants : carbonate de cliaux, sulfate de
chaux, carbonate’ de magnésie, chlorure de sodium, sulfate de soude [Loc eit
p. 79].
Silice Si O2 3.6 m&
Chlorure de sodium Na Cl 2.0
Sulfate de sodium Na2 SO4 10.4
Sulfate de potassium K2 SO4 3.7
Sulfate de calcium Ca SO4 49.8
Carbonate de calcium Ca CO3 74.9
Carbonate de magnésium Mg CO3 20.4
Total des sels minéraux dissous 164.8
Matières organiques, pertes et divers 10.2
Total des matières dissoutes ou du
résidu fixe 175.0
Chaque chimiste pourra combiner à sa manière le tableau des sels.
Dans l’état actuel de la science, il répond suffisamment à la réalité des
faits connus.
Ce sont les chiffres que nous admettrons comme probables et représentant,
jusqu’à nouvel avis, là composition chimique des eaux du
Léman.
III. Discussion des résultats d’analyse.
En étudiant les chiffres et tableaux ci-dessus, provenant de tant de
chimistes divers, il me paraît qu’on peut en tirer trois conclusions que
nous aurons à discuter.
1° Les résultats généraux sont assez concordants.
2° Il y a des différences importantes entre les séries données par les
divers auteurs.
3« Entre les analyses faites par le,môme auteur, il y a des différences
sensibles.
1° ConcovdcancG ygyigtoXg des vésiiltats d'cmcdysG. Je crois pouvoir établir
en thèse générale que la composition chimique du lac, considérée
dans son ensemble, doit être invariable, ou que, si elle varie, cette variation
doit être progressive et très lente. Mon raisonnement est le suivant
: Le volume des eaux du Léman est énorme : 89 milliards de
mètres cubes. Dans un tel volume, une variation de 1 milligramme par