Si nous remplissons un ballon de l’eau de surface d’un lac et que nous l’exposions
à une température supérieure à celle du lac, nous voyons, au bout d’un
certain temps, lorsque l’équilibre des températures s’établit, des bulles gazeuses se
dégager. Mais, et c’est là un point très important, le dégagement est loin d’être
instantané. J’ajouterai que celui de l’acide carbonique lié aux carbonates est extrêmement
lent. On peut conserver longtemps une eau sursaturée de bicarbonate de
chaux sans qu’aucun dépôt se produise. Ainsi j ’ai fait passer pendant huit heures
un courant d’air, puisé dans un jardin au-dessus de Thonon, à travers un ballon
rempli d’eau du fond du lac de Nantua, eau fortement sursaturée de carbonate de
chaux par rapport à la tension de l’acide carbonique de l’atmosphère, et je n’ai
obtenu aucun précipité; l’eau avait la même teneur après qu’avant l’opération'.
On peut donc recueillir simplement l’eau de surface d’un lac dans un ballon
qu’on s’arrangera ensuite pour fermer hermétiquement avant que l’échappement des
gaz dissous ait eu le temps de se produire, tout en permettant à la dilatation du
liquide de s’exercer. Mais, pour l’eau des profondeurs, n’y a-t-il pas quelque précaution
spéciale à prendre ?
Parmi les bouteilles employées généralement pour récolter les échantillons
d’eau au fond des lacs ou des mers, les unes (bouteilles de Mill, de Buchanan) ne
sont pas construites pour résister à la pression. Dans la bouteille de Mill, l’obturation
se fait au moyen d’une enveloppe cylindrique légèrement effilée qui vient
peser sur un disque de caoutchouc ; à mesure que l’eau se décomprime pendant la
remontée de la bouteille, elle s’échappe entre l’enveloppe cylindrique et le caoutchouc.
Dans ces conditions, si, comme on l’a cru longtemps, l’eau des profondeurs
renfermait des gaz en quantité considérable, nous n’aurions aucun moyen sûr de
nous en apercevoir ; car les gaz pourraient s'échapper en même temps que l’excès
d’eau résultant de la décompression. Les autres bouteilles (celles du Travailleur et
du Vôringen, par exemple8) ne peuvent résister à la pression que par l’intermédiaire
de joints, de soupapes ou de robinets; dans ces conditions, pour des variations
de pression qui atteignent 30 atmosphères, comme au lac de Genève, des
fuites paraissent bien difficiles à éviter.
A la vérité l’accumulation des gaz dans les profondeurs des lacs est très invraisemblable.
Car cette eau des profondeurs a été apportée dans le lac soit parla pluie,
soit par des affluents dont les eaux, tout au moins celles des affluents superficiels,
ne renferment pas un excès de gaz. De plus, la même eau ne séjourne pas indéfiniment
au fond des lacs; les courants et les convections thermiques verticales la
1. Ce r é su lta t p a ra ît ê tr e en co n tr a d ic tio n a v e c le s lo is d e S ch loe sin g. Il s ’ex p liq u e p rob ablem en t
par c e fa it q u e , la p r e ssio n d e l’ea u d ont j e d isp o sa is p o u r ap p e le r l’a ir au m o y en d’u n e tr om p e étant
a sse z fa ib le , le p assage d e c e t a ir à tr a v ers l e b a llon s e fa isa it trop len tem e n t pour q u e la d écom po sitio
n d u b ic a rb ona te eû t lieu p en d a n t la d ur ée d e l ’ex p é r ien c e . La m êm e e x p é r ien c e , r ép é té e sur l’eau
du la c d e C h a ille x on, a d onn é u n r é su lta t an a lo gu e.
2 . Voir T h o u l e t , Océanographie sta tiqu e, p , 199 e t 204.
renouvellent assez fréquemment; les gaz ne peuvent pas s’y amasser comme au
fond d’une grotte où l’air ne circule point. Enfin le dégagement des gaz d une eau
fortement gazeuse ne se fait jamais instantanément; lorsque nous ouvrons une
bouteille d’eau minérale ou de vin de Champagne, il se passe parfois plusieurs
heures avant que les dernières bulles emprisonnées finissent par disparaître. Si donc
l’eau que nous ramenons des profondeurs dans une bouteille de Mill était fortement
chargée de gaz, ceux-ci n’auraient
probablement pas le temps
de s ’échapper entièrement pendant
les quelques minutes que
l’instrument met à remonter;
en transvasant cette eau dans un
ballon, nous devrions voir le
dégagement continuer pendant
quelque temps encore. Or, nous
n’observons rien de semblable,
tout se passe comme pour l’eau
que nous prenons à la surface.
Cependant il m’a paru qu’une
preuve directe ajoutée à ces raisonnements
ne serait pas sans
utilité. J’ai donc cherché à puiser
l’eau du fond des lacs dans un
appareil qui ne permît à cette
eau aucun contact ni avec les
couches supérieures ni avec
l’atmosphère, et, avec la collaboration
de M. A. Le Royer,
professeur au collège de Genève,
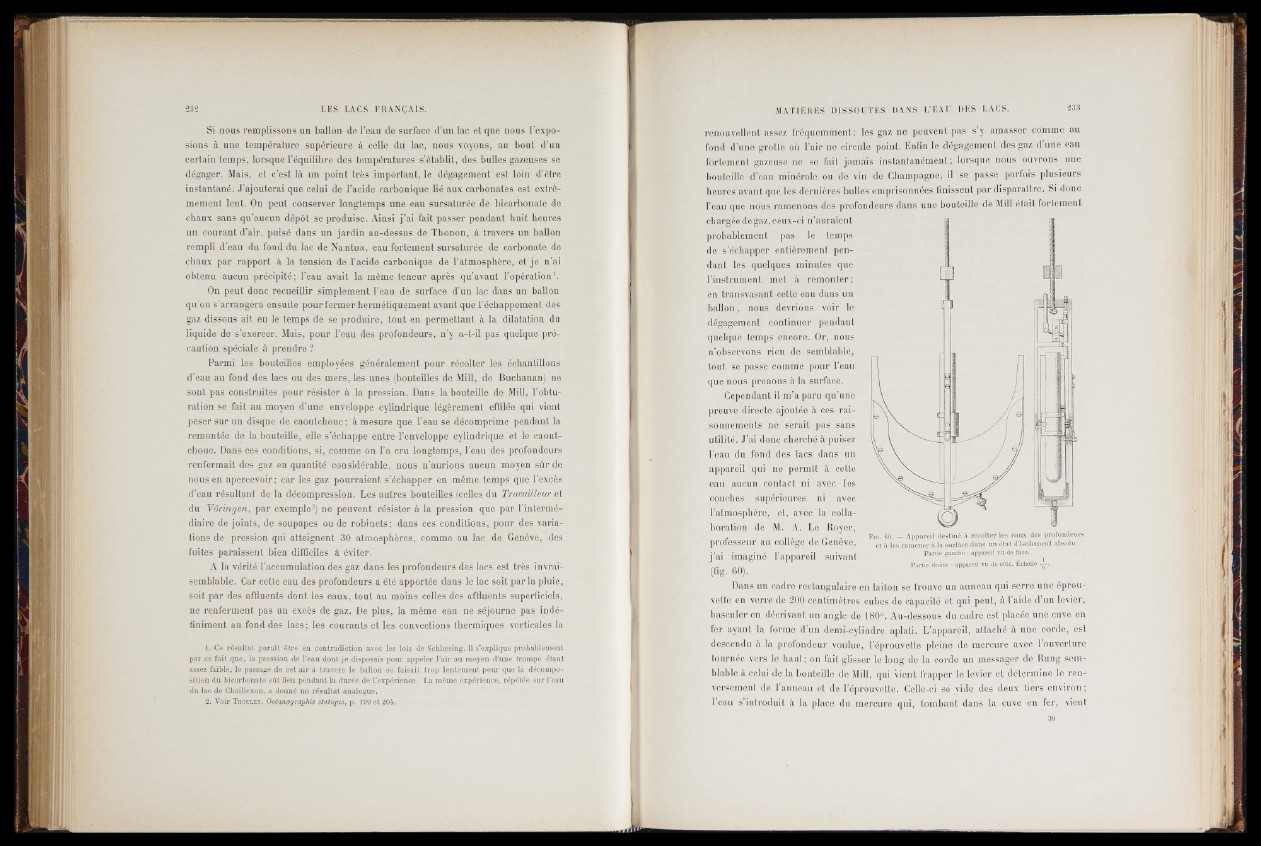
j’ai imaginé l’appareil suivant
(fig- 60).
F ig. 60. — A p p a r e il d e s t in é à r é c o l t e r le s e a u x d e s p r o fo n d e u r s
e t à le s r am e n e r à l a s u r f a c e d a n s u n é t a t d ’i s o lem e n t a b s o lu .
Dans un cadre rectangulaire en laiton se trouve un anneau qui serre une éprouvette
en verre de 200 centimètres cubes de capacité et qui peut, à l’aide d’un levier,
basculer en décrivant un angle de 180°. Au-dessous du cadre est placée une cuve en
fer ayant la forme d’un demi-cylindre aplati. L’appareil, attaché à une corde, est
descendu à la profondeur voulue, l’éprouvette pleine de mercure avec l’ouverture
tournée vers le haut ; on fait glisser le long de la corde un messager de Rung semblable
à celui de la bouteille de Mill, qui vient frapper le levier et détermine le renversement
de l’anneau et de l’éprouvette. Celle-ci se vide des deux tiers environ ;
l’eau s’introduit à la place du mercure qui, tombant dans la cuve en fer, vient
30
P a r tie gauche : appa re il v u de face,
a rtie droite : appareil vu de côté. Echelle —-.